
Základní princip enzymové reakce
Historie matematického popisu modelů enzymové kinetiky je spojena především se jmény Leonora Michaelise (1875-1949), německého biochemika, fyzikální chemika a fyzika, a Maud Mentenové (1879-1960), kanadské lékařky, působící od roku 1912 v Berlíně.
Enzymy umožňují přeměnu molekul jedné látky na molekuly látky jiné. Vstupní látka, která se má transformovat, se nazývá substrát a látka, která reakcí vzniká, se nazývá produkt, budeme pro ně proto užívat zkratky S a P. V typických reakcích enzymy (zkratka E) urychlují (katalyzují) proces přeměny látek tím, že se na sebe váží substrát za vzniku tzv. komplexu enzym-substrát (označení C, někdy též ES). Tento komplex C se pak může za určitých podmínek rozpadnout na volný enzym E a produkt P. Tato přeměna však může také selhat v tom smyslu že komplex C se rozpadne zpět na volný enzym E a substrát S. Předpokládáme tedy, že vázání enzymu na substrát je reverzibilní, zatímco příp. rozpad komplexu na E a P je ireverzibilní. Kinetické schéma této enzymové reakce je
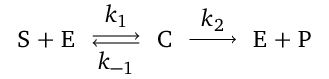 |
(14) |
Rychlostní konstanty a
jsou pak po řadě spojeny se vznikem komplexu (syntéza), rozpadem komplexu na substrát (analýza) a s formováním produktu z komplexu (analýza). Konstanta
je, stejně jako konstanta
spojena s analýzou komplexu C, má tedy i stejnou jednotku, s-1.
Použitím principu law of mass action lze pak pro koncentrace jednotlivých látek, tedy komplexu enzym-substrát, volného enzymu,
substrátu,
a produktu
jakožto funkci času
psát čtyři diferenciální rovnice
|
|
|
|
|
|
|
|
|
|
|
spolu s počátečními podmínkami
|
|
(19) |
Na začátku reakce je množství produktu nulové, v praxi je často nulová i počáteční koncentrace komplexu
Při známých konstantách a hodnotách počátečních koncentrací
lze vývoj koncentrací určit numericky. Pro numerické výpočty a grafická zobrazení budeme v celé této kapitole uvažovat následující hodnoty parametrů:
|
|
(20) |
Numericky získaná řešení počáteční úlohy Enzymová kinetika (15) - (19) s těmito parametry jsou vykreslena v obr. Enzymová kinetika 1 a Enzymová kinetika 2.
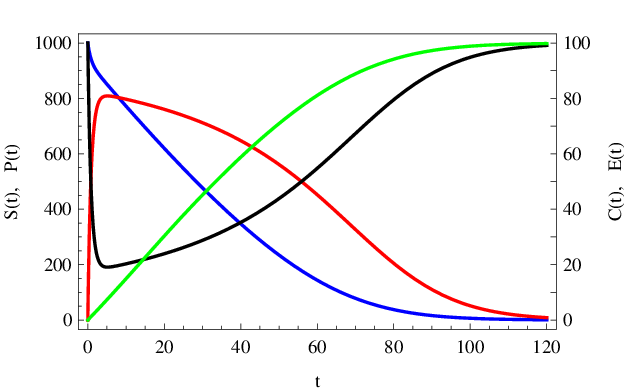 |
|
Obr. 1. Numericky spočítané průběhy (čas v sekundách) koncentrací (mol dm-3) substrátu S(t) (modře), produktu P(t) (zeleně), volného enzymu E(t) (černě) a komplexu enzym-substrát C(t) (červeně) podle kinetického schématu Enzymová kinetika (14) s parametry Enzymová kinetika (20). Koncentrace C(t) a E(t) mají odlišné škálování podle měřítka na pravé straně grafu.
|
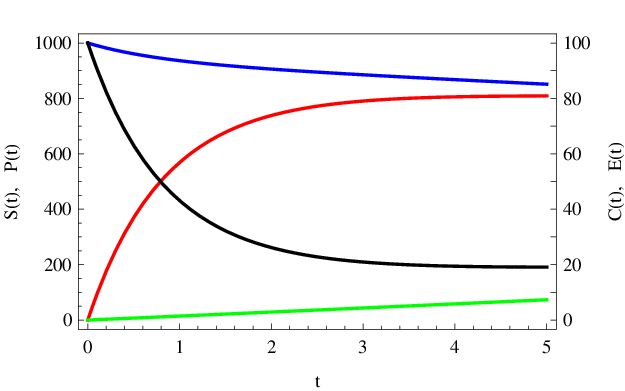 |
|
Obr. 2. Detail z obr. Enzymová kinetika 1 zobrazující koncentrace v počáteční fázi reakce.
|
Vidíme, že koncentrace substrátu s rostoucím časem klesá, a to přibližně exponenciálně, a koncentrace
produktu roste. Koncentrace
volného enzymu nejdříve klesá, poté se zvolna vrací k počáteční koncentraci
Koncentrace
komplexu naopak nejdříve roste a poté zvolna klesá k nule. Pro
dojde ke stabilizaci systému, všechen substrát bude postupně přeměněn na produkt a enzym po ukončení této reakce zůstane opět výhradně ve volné formě.
Pro analýzu úlohy Enzymová kinetika (15)-(19) bychom kromě numerických výsledků potřebovali i přesná řešení v analytickém tvaru. Jejich výpočet je však i pro uvažovanou reakci velmi složitý, běžnými postupy systém vyřešit neumíme, systém diferenciálních rovnic totiž není lineární.
Ukážeme proto tzv. quasi-steady-state aproximaci, která poskytuje jednoduchý a užitečný, ale přitom relativně přesný, pohled na interakci enzym-substrát-produkt. Kromě odvození přibližného řešení systému diferenciálních rovnic ukážeme i obecný postup, jak složitý systém zjednodušit na aproximovaný systém a jak zároveň zhodnotit přesnost aproximace a ověřit podmínky pro její platnost.
Než se budeme aproximaci věnovat, všimněme si ještě některých závislostí v úloze Enzymová kinetika (15)-(19). Koncentrace produktu vystupuje pouze v rovnici Enzymová kinetika (18) a k jejímu výpočtu potřebujeme znát průběh koncentrace
komplexu. Nejdříve je tedy nutné vyřešit systém první tří diferenciálních rovnic pro koncentrace
koncentraci produktu
pak nalezneme integrováním koncentrace komplexu,
|
|
(21) |
Sečtením rovnic Enzymová kinetika (15) a Enzymová kinetika (16) dostaneme
|
|
(22) |
tzn. součet koncentrací a
je konstantní, podle Enzymová kinetika (19) rovný
|
|
(23) |
Enzym se tedy v reakci vlastně vyskytuje ve dvou formách: jako volný E a jako vázaný v komplexu C. To je patrné i na časových průbězích koncentrací a
v obr. Enzymová kinetika 1 a Enzymová kinetika 2. Z Enzymová kinetika (23) vyjádříme koncentraci
a dosadíme do rovnic Enzymová kinetika (15) a Enzymová kinetika (17). Tím nám v systému zůstanou pouze dvě diferenciální rovnice
|
|
(24) |
|
|
(25) |
pro koncentrace a
s počátečními podmínkami
Součet koncentrací substrátu a produktu však obecně konstantní není. Všechen substrát se sice přemění na produkt, ale součet jejich koncentrací je roven
pouze na začátku a na konci reakce, jak je patrné z následujícího obrázku.
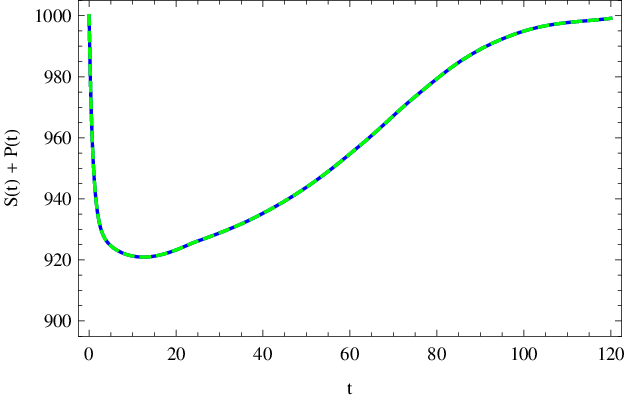 |
|
Obr. 3. Součet koncentrací ( mol dm-3) S(t) + P(t) substrátu a produktu v čase (sekundy) podle kinetického schématu Enzymová kinetika (14) s parametry Enzymová kinetika (20).
|




